Aroa, consultora de Life Sciences en ALTEN, es experta en “Validación de Sistemas Informatizados y Control de Calidad”. En esta ocasión, nos habla sobre la necesidad actual de validar los sistemas informatizados en la industria regulada.
¿Por qué existe la necesidad de validar los sistemas informatizados en la industria farmacéutica?
La industria farmacéutica es una industria regulada, la cual se ve obligada a cumplir con una serie de requisitos normativos muy exigentes, con altos estándares técnicos y de calidad. Por lo tanto, es de obligado cumplimiento que la totalidad de los sistemas informatizados a implantar se sometan a una validación, más o menos extensa, en función de la categoría de estos.
La Food and Drug Administration (FDA) considera que la validación del software es “la confirmación, mediante el examen y la presentación de pruebas objetivas, de que las especificaciones del software se ajustan a las necesidades del usuario y a los usos previstos, y de que los requisitos particulares implementados a través del software pueden cumplirse de manera consistente”.
Atendiendo a la parte 11, de la guía 21, del código de regulaciones generales de la FDA, los sistemas informatizados utilizados para crear, modificar y mantener registros electrónicos, y para gestionar las firmas electrónicas también están sujetos a los requisitos de validación. Dichos sistemas informáticos deben ser, por lo tanto, validados para garantizar la precisión, fiabilidad, rendimiento previsto y la capacidad de discernir registros no válidos o alterados.
La importancia, por tanto, de la validación de sistemas informatizados, radica en cumplir con todos los estándares y la normativa exigida, además de aportar diferentes beneficios al sector farmacéutico, entre los que destacan:
- Asegurar la calidad e integridad de los datos: Los datos deben cumplir con la regla ALCOA+ (Atribuible, Legible, Contemporáneo, Original, Preciso, Completo, Consistente, Duradero y Disponible) durante todo su ciclo de vida.
- Trazabilidad de los procesos: Evitar la pérdida de información en el transcurso del proceso.
- Estandarización de procesos: Flujos de trabajo definidos que minimizan los errores.
- Gestión de la calidad y mejora continua: La trazabilidad facilita la corrección de errores, la introducción de mejoras y la constante revisión de los procesos.
Por consiguiente, el proceso de validación de sistemas informatizados es un requerimiento para cumplir con las buenas prácticas de fabricación (GMP – Good Manufacturing Practises ) y es clave a la hora de garantizar la calidad de los procesos.
¿Cómo saber qué categoría tiene un sistema informatizado?
La guía para validación de sistemas informatizados, sujetos a buenas prácticas más extendida y aplicada por la industria farmacéutica, es la GAMP (Good Automated Manufacturing Practice), cuya versión actual es el número cinco y la cual está publicada por el ISPE (International Society for Pharmaceutical Engineering).
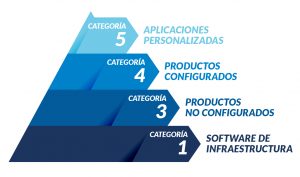
Las categorías GAMP se introdujeron originalmente para proporcionar una evaluación inicial en cuanto a los requisitos/entregables de validación. En la anterior versión, GAMP 4, existían cinco categorías de software, las cuales han sido reducidas a cuatro en la versión actual. La categoría 1 corresponde al caso de software menos complejo y la categoría 5 al más complejo.
¿Qué tipo de sistemas son susceptibles de ser validados en la industria farmacéutica?
Los sistemas informatizados susceptibles de ser validados en la industria farmacéutica son todos aquellos que gestionen parámetros de funcionamiento que puedan afectar a la calidad de los productos finales, además de sistemas de gestión de documentación o sistemas que gestionen o manejen datos relevantes.
Entre otros, se encuentran:
- Sistemas de planificación de recursos empresariales (ERP)
- Electronic Batch Record (EBR)
- Sistemas de gestión de almacén (SGA)
- Gestión de sistemas de laboratorio, (LIMS)
- Sistemas de gestión documental, (EDMS)
- Sistemas de control de la producción, (MES)
- Sistemas de supervisión, control y adquisición de datos (SCADA)
- Hojas Excel
[gravityform id=”2″ title=”true” description=”true” /]









